Fターム[4C084ZC02]の内容
蛋白脂質酵素含有:その他の医薬 (348,545) | 医薬用途・機能・機作・対象・その他 (30,064) | 生体機能への作用で特定された医薬 (18,288) | 生体内生理活性物質様薬 (9,333)
Fターム[4C084ZC02]の下位に属するFターム
ホルモン様剤 (2,453)
プロスタグランジン様剤 (69)
抗ヒスタミン剤 (140)
抗セロトニン剤 (77)
ブラジキニン様剤 (14)
アンジオテンシン様剤 (75)
酵素活性・賦活剤 (430)
酵素阻害剤 (3,418)
Fターム[4C084ZC02]に分類される特許
2,601 - 2,620 / 2,657
プロトン感受性Gタンパク質共役型受容体およびそのDNA配列
本発明は、ある種のGタンパク質共役型受容体(GPCR)、特にOGR1、GPR4およびTDAG8(TDAG8はGPR65とも呼ばれる)ポリペプチド、およびそのようなGPCRポリペプチドをコードするポリヌクレオチドの新規に認められた有用性、診断におけるそれらの使用、該GPCRに対するアゴニストまたはアンタゴニストである化合物を同定する方法、ならびにそのようなポリペプチドおよびポリヌクレオチドの生産に関する。 (もっと読む)
RNAインターフェラーゼおよびその使用方法
本発明は、本明細書中でmRNAインターフェラーゼと呼ばれるエンドリボヌクレアーゼ活性を示す新規の酵素ファミリーの発見に関する。したがって、本発明の新規の所見は、mRNAインターフェラーゼの核酸配列およびアミノ酸配列ならびにその組成物を使用して利益をもたらすことができる新規の適用を示す。本発明はまた、mRNAインターフェラーゼ活性を調節することができる化合物/薬剤を同定するためのスクリーニング法およびこのような化合物/薬剤の使用方法を含む。mRNAインターフェラーゼの核酸配列および/またはアミノ酸配列、mRNAインターフェラーゼ活性適合緩衝液、および取扱い説明書を含むキットも提供する。 (もっと読む)
延長された治療ウインドウを有する、応答性細胞、組織および器官の保護、回復および増強のための組織保護サイトカイン
すでに承認済の治療薬の治療ウインドウ外の時点で投与するとき、哺乳動物における応答性細胞、組織、器官もしくは身体部分の機能または生存能力を保護する、もしくはこれらの機能を回復するための、エリスロポイエチンまたは組織保護サイトカインを含む医薬組成物の方法および使用が提供される。 (もっと読む)
増加した活性を有する修飾されたヒト酸性スフィンゴミエリナーゼおよびその製造方法
酸性スフィンゴミエリナーゼ(ASM)の酵素活性の欠損は、ニーマン-ピック病をもたらす。ASMのC末端システイン残基の遊離チオール基の活性を除去する様々の修飾は、いずれもこの酵素の比活性を実質的に増加させる。この残基の活性を変化させるために用いられる方法には、この残基を除去または変化させるための部位特異的変異導入、この残基を除去するためのASMの酵素的分解、銅により促進されるASMの(末端システイン残基を介した)二量体化、およびこの残基の遊離チオール基の化学的修飾が含まれる。 (もっと読む)
抗癌剤としてのヘテロアリール縮合ピリミジニル化合物
本発明は、ヘテロアリール縮合ピリミジニル化合物、それらの薬学的に受容可能な塩およびプロドラッグ;単独でまたは少なくとも1種の追加治療薬と併用していずれかでの薬学的に受容可能なキャリアとヘテロアリール縮合ピリミジニル化合物とを含有する組成物に関する。本発明はまた、増殖疾患の治療または予防における単独でかまたは少なくとも1種の追加治療薬と併用してかのいずれかでの該ヘテロアリール縮合ピリミジニル化合物を使用する方法に関する。 (もっと読む)
ケモカイン結合タンパク質およびその使用方法
本発明は、THAPドメインを含むTHAPファミリーの遺伝子およびタンパク質と、疾患の診断および治療、ならびに疾患の治療のための分子の同定におけるその使用とに関する。本発明はまた、ケモカインに対する核受容体としてのTHAPファミリータンパク質のようなTHAP型ケモカイン結合物質の使用、および転写、細胞増殖、および細胞分化を調節(刺激または阻害)する方法、ならびにTHAP−ケモカイン相互作用を調節する化合物を同定する方法にも関する。 (もっと読む)
IL−2の副作用の緩和方法
新規多型(±)-7-[3-(4-アセチル-3-メトキシ-2-プロピルフェノキシ)プロポキシ]-3,4-ジヒドロ-8-プロピル-2-カルボン酸を開示する。本化合物は、80〜82℃の高融点を有し、ロイコトリエンB4アンタゴニスト(「LBA」)である。本化合物は、IL-2治療の逆事象(例えば血管漏出症候群)を軽減するために有用である。IL-2と組み合わせた本化合物の投与は、IL-2の逆事象を軽減し、かつ対象に対するLBA投与の有利な効果を維持し又は亢進すると同時に、LBAを用いる副作用を同時に緩和する。本方法は、IL-2治療を受ける対象にLBA、好ましくは新規多型のある量を投与であって、当該投与量はLBAが治療計画に渡って特定範囲に維持される、投与を含む。また、添付の治療指示書と共に新規多型の組成物を含む製品を開示する。また、新規多型の医薬組成物の製造方法及び多型そのものの製造方法を開示する。 (もっと読む)
キネシン活性の調節因子を同定するための方法
第一の局面において、標的タンパク質の調節因子をスクリーニングするための方法を提供し、この方法は、標的タンパク質を候補因子と接触させる工程;およびこの候補因子がその標的タンパク質の活性を調節するか否かを決定する工程;を包含し、その標的タンパク質は、KIF14(配列番号2)またはKIF14モータードメイン(配列番号3)に対して80%より高いアミノ酸配列同一性を有する配列を含む。第二の局面において、本発明は、細胞増殖を調節する方法を提供し、この方法は、細胞に、有効量の標的タンパク質の活性の調節因子を投与する工程を包含する。この局面のいくつかの実施形態は、細胞過剰増殖障害(例えば、癌)を有する被験体を処置するための方法を提供する。第三の局面において、本発明は、標的タンパク質の活性のインヒビターを用いる処置のための候補被験体を同定するための方法を提供する。 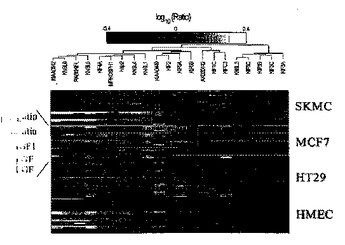 (もっと読む)
(もっと読む)
組成物の組み合わせの多次元評価システムおよび方法
本発明の実施態様の目的は、構成素アレイ由来の構成素組成物の組み合わせを含む分析アレイを作製するための方法と器具である。本発明のある実施態様では、組み合わせ組成物を評価して組み合わせ効果を有する組み合わせが特定される。本発明の他の実施態様の目的は、構成素アレイを様々な構成で作製し、分析アレイの生成を促進することである。この様な実施態様には:対応する組成物と分析対照セットを有する構成素アレイを作製する工程と;基点位置の固有セットと派生位置の対応するセットを有する構成素アレイを作製する工程と;構成素組成物に利用される濃度を変化する工程と;仮想空間分析アレイに対応する分析アレイを構成する工程とが含まれる。本発明の他の実施態様の目的は、分析アレイ中の組み合わせ組成物の活性を評価するシステムおよび方法である。 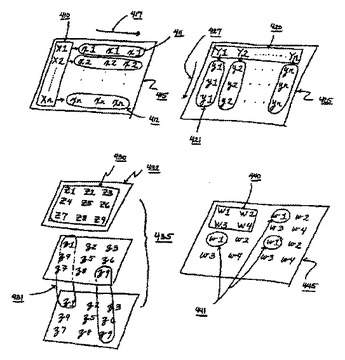 (もっと読む)
(もっと読む)
系統発生的に関連のある配列のライブラリー
本発明は、系統発生的に関連のある配列のアッセイ法および可能な核酸またはアミノ酸配列の組み合わせのセットを作成する方法を含む。配列はアラインメントを作成するために解析され、系統発生的に関連のある配列のセットが選択される。選択された系統発生的に関連のある配列のアラインメントにおいて各位置を占めている観察される残基またはインデルが同定され、この情報が配列の組み合わせのセットを作成するために用いられ、ここで可能な配列の組み合わせ(核酸またはポリペプチド)であるこのセットは、各位置で同定された観察される残基またはインデルの集合から構成される。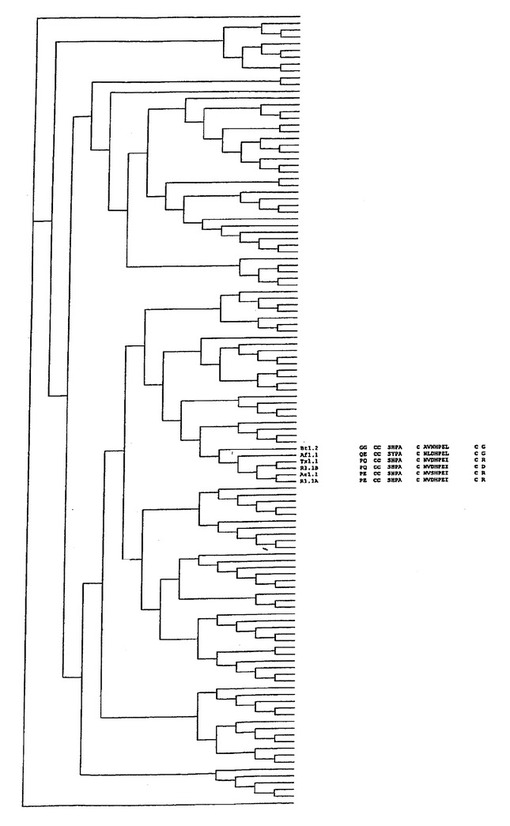
 (もっと読む)
(もっと読む)
有効性を高めたケモカインレセプタ結合複素環化合物
本発明は、3つのペンダント基に囲まれたコア窒素原子からなる複素環化合物を提供する。これらのペンダント基のうちの2つは、好ましくは、ベンズイミダゾリルメチルおよびテトラヒドロキノリルであり、そして第3のペンダント基はNを含み、そして必要に応じてさらなる環を含む。この化合物は、ケモカインレセプター(CXCR4およびCXCR5を含む)に結合し、そしてヒト免疫不全ウイルス(HIV)による標的細胞の感染に対する保護効果を示す。 (もっと読む)
VEGFアンタゴニストの使用による角膜移植拒絶を処置する方法
本発明は、血管内皮増殖因子(VEGF)をブロックまたは阻害し得る薬剤の投与が、角膜移植拒絶を予防するという知見に、部分的に基づく。角膜移植拒絶を予防、軽減、または処置することを必要とする被験体において、角膜移植拒絶を予防、軽減、または処置して移植片生着を改善する方法が、提供される。本方法は、血管内皮増殖因子(VEGF)をブロックまたは阻害し得る薬剤を投与する工程を包含する。本方法は、移植される角膜のレシピエントであるヒト被験体において角膜移植拒絶を阻害または予防することにとって有用である。 (もっと読む)
補体阻害剤
【解決手段】本発明は、補体古典経路と補体代替経路の両方を阻害する補体阻害剤に関する。本発明は特に、補体古典経路と補体代替経路の両方を阻害する、吸血性節足動物の唾液腺由来の補体阻害剤に関する。更に本発明は疾患の治療及び予防におけるこのような補体阻害剤の使用に関する。 (もっと読む)
ABT−751による持続投与レジメン
抗癌剤N−(2−((4−ヒドロキシフェニル)アミノ)ピリド−3−イル)−4メトキシベンゼンスルホンアミド(ABT−751)を含有する組成物、チューブリンβ−サブユニットのコルチシン部位と結合する前記薬剤による持続経口投薬スケジュール、及び持続投薬スケジュールを使用する疾患の治療方法を開示する。 (もっと読む)
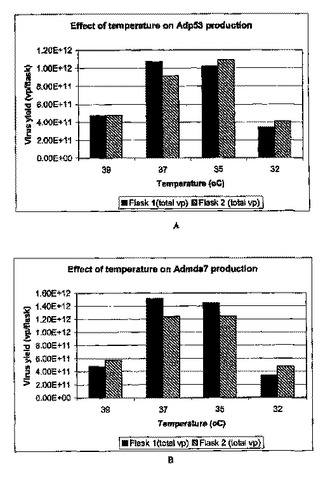
アデノウイルスベクター産生のための方法および組成物
本発明は、細胞培養系で成長した場合のアデノウイルスの収率を改善する必要性に取り組む。特に、アデノウイルスについて、細胞培養系における37℃未満の感染温度の使用により、アデノウイルスの収率が改善されることを証明した。さらに、宿主細胞がバイオリアクター中で成長した場合、新鮮な培地およびアデノウイルスでの宿主細胞の希釈によるアデノウイルス感染の開始によって、アデノウイルスの収率が改善されることを証明した。37℃未満の感染温度を使用したアデノウイルスの産生および精製方法を開示する。宿主細胞をバイオリアクター中で成長させ、宿主細胞を新鮮な培地およびアデノウイルスで希釈することによってアデノウイルス感染を開始させるアデノウイルスの産生および精製方法も開示する。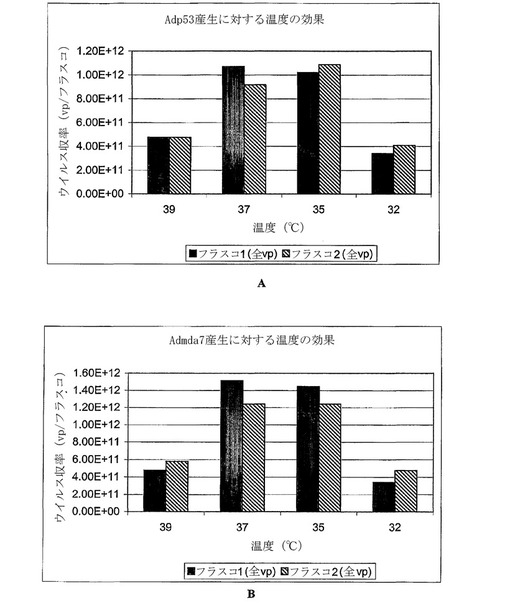
 (もっと読む)
(もっと読む)
Gタンパク質結合受容体オリゴマーに関する物質及び方法
この発明は、Gタンパク質結合受容体(GPCR)オリゴマーに関する物質及び方法を提供する。Gタンパク質と結合した2つ以上のGPCRの複合体を提供する。また、GPCRとGタンパク質を含む融合タンパク質、核酸、発現ベクター及び宿主細胞を提供する。また、本発明の複合体及び融合タンパク質を製造する方法を提供する。 (もっと読む)
ペルオキシソーム増殖因子活性化受容体のリガンドとしてのN−アシル窒素ヘテロ環
式(I)
【化1】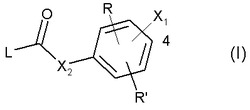
の化合物は、ペルオキシソーム増殖因子活性化受容体(PPAR)に結合する薬剤を提供する。従って、本発明の化合物は、哺乳動物のPPAR受容体活性により仲介される状態の処置に有用である。かかる状態には、脂質代謝異常、高脂血症、高コレステロール血症、アテローム性動脈硬化症、高トリグリセリド血症、心不全、心筋梗塞、血管疾患、心臓血管疾患、高血圧、肥満症、炎症、関節炎、癌、アルツハイマー病、皮膚疾患、呼吸器疾患、眼疾患、炎症性腸疾患、潰瘍性大腸炎、クローン病、ならびに1型および2型糖尿病、およびX症候群などの耐糖能異常、高血糖およびインスリン耐性が関与する状態が含まれる。 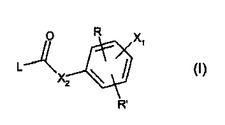 (もっと読む)
(もっと読む)
ウロキナーゼ阻害剤としてのヒドロキシアミジン化合物およびヒドロキシグアニジン化合物
本発明は、高い生物学的利用能および経口投与性を有するウロキナーゼ−プラスミノゲン−アクチベーター(uPA)を抑制するための新規の化合物ならびにウロキナーゼおよび/またはウロキナーゼ受容体に関連する疾患、たとえば腫瘍および転移を治療するための治療作用物質としての該化合物の使用に関する。本発明は特にヒドロキシアミジン基またはヒドロキシグアニジン基を有する化合物に関する。式(I)または式(II)において、Eは式(III)、式(IV)からの基を表す。 (もっと読む)
安定なペプチド及びポリペプチドアナログ治療剤
本発明は、蛋白質分解に対して耐性のあるペプチド及びポリペプチドアナログの組成物、その医薬としての使用及びその製造方法に関する。 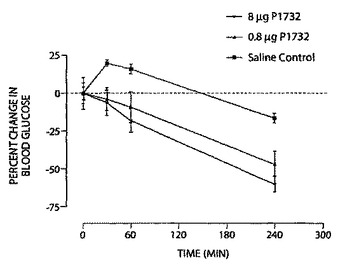 (もっと読む)
(もっと読む)
γ−セクレターゼ阻害剤のスクリーニング方法
本発明は、γ−セクレターゼ活性を決定するための改善されたプロセス、本プロセスの個々の構成要素、および、本プロセスの使用に関する。本発明は、γ−セクレターゼ活性を決定するため、および、γ−セクレターゼ、γ−セクレターゼのサブユニットタンパク質、または、γ−セクレターゼ様のプロテイナーゼを検出するための、改善されたプロセスに関する;本プロセスの特定の実施形態は、一方では、γ−セクレターゼ、または、γ−セクレターゼ、γ−セクレターゼのサブユニットタンパク質もしくはγ−セクレターゼ様のプロテイナーゼをコードするcDNAの同定プロセスに関し、一方では、γ−セクレターゼ、γ−セクレターゼのサブユニットタンパク質、または、γ−セクレターゼ様のプロテイナーゼの活性を阻害することができる物質の同定プロセスに関する。このような物質は、例えばアルツハイマー病の治療のための医薬活性化合物として用いることができるために特に重要である。 (もっと読む)
2,601 - 2,620 / 2,657
[ Back to top ]